日本将特殊医学用途配方食品(FSMP)称为病人用特殊用途食品,属于特殊用途食品的一类。《健康增进法》规定特殊医学用途配方食品实行审批制管理模式,即产品上市前需要通过日本厚生劳动省批准许可,与中国的注册批准制度类似。截至2023年7月14日,中国已经批准的特医食品有124款(不含已注销产品,有7款产品暂未收录入特殊食品查询平台,数据来源于网络,供参考),那么日本同期已经许可的此类产品有多少款,主要为哪些类型的产品?下面和食品伙伴网一起来了解下吧。
01.病人用特殊用途食品分类
日本规定病人用特殊用途食品分为标准型和个别评估型两类。
标准型包括低蛋白质食品、去过敏原食品、无乳糖食品、综合营养食品、糖尿病患者用组合食品、肾病患者用组合食品、口服补水液。日本厚生省根据对应的标准对所申报的产品审核与审批,时间较短,程序简单。
个别评估型病人用特殊用途食品中营养成分与标准型相比进行了调整,需要提供相应材料对这些调整进行说明,消费者厅组织专家委员会对产品的适宜性及安全性进行全面的评价,结合相关意见进行审核,通过评估后方可审批上市,时间长,审批流程相对复杂。
我国特医食品按照适用年龄可以分为两个类别,即适用于0~12月龄婴儿的特殊医学用途婴儿配方食品(以下简称特医婴配)和适用于1岁以上人群的特医食品,后者又可进一步分为全营养配方食品、特定全营养配方食品以及非全营养配方食品。常见的特医婴配食品如无乳糖或低乳糖配方、乳蛋白深度水解或氨基酸配方、早产/低出生体重婴儿配方等。非特医婴配食品分为全营养配方、特定全营养配方和非全营养配方三大类。
日本和中国的产品种类有所不同,相同的是都按照适用人群对营养素或膳食的特殊需要进行了细分类型的区分。
02.病人用特殊用途食品许可情况
食品伙伴网对日本消费者厅公布的特殊用途食品标识许可明细进行梳理,截至2023年8月7日,日本共批准了51款病人用特殊用途食品,详情见表1。
表1 日本病人用特殊用途食品许可情况
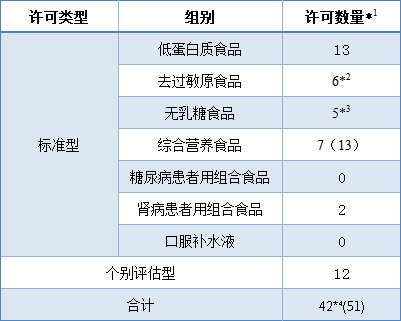
*3包括3个被允许用于去过敏原的食品。
*4关于作为去除过敏原食品和无乳糖食品许可的3件,因为都在各自的食品组别中进行了计算,所以许可标示的数量是42件。
中国已获批的124款特医食品中,特医婴配产品39款,非全营养类产品46款,全营养类产品38款,特定全营养类产品1款(肿瘤全营养配方)。已获批产品的详情见表2。
表2 中国特医食品批准情况
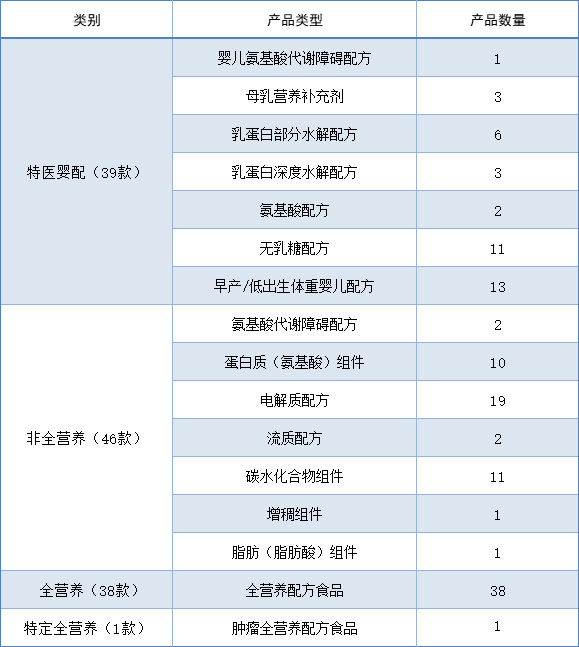
从批准的产品数量上看,中国的特医食品起步虽然比较晚,但是发展还是比较迅速的。日本因管理模式比较严格等原因,特病人用特殊用途食品虽然历史相对悠久,但是数量并没有十分突出。
03.2023年上半年批准的病人用特殊用途食品
根据日本消费者厅公布的特殊用途食品标识许可品种一览表,查询到日本2023年上半年获批的病人用特殊用途食品共有2款,其详情见表3。
表3 2023年上半年病人用特殊用途食品批准情况
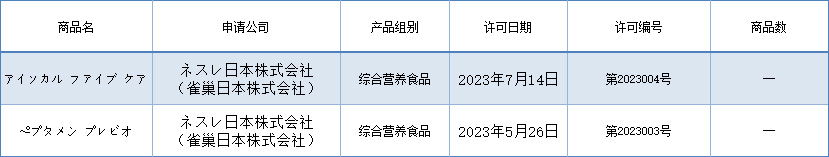
从上半年许可的数量上看,2023年上半年许可的产品比较少,查询特殊用途食品许可目录看出,被许可的主体基本是大型的食品或者药品公司,比如佐藤食品株式会社、朝日集团食品株式会社、明治株式会社、日本生物科技株式会社、雀巢日本株式会社、大冢制药株式会社等大型企业。这也反映出日本对病人用特殊用途食品许可和管理都是十分严格的,获得许可并不容易。
04.小结
日本对于病人用特殊用途食品的管理制度相对我国时间较长,产品种类比较全面,对我国相关方开展同类产品的研究开发、申报审批等具有一定的借鉴意义。
素材来源网络,如侵删