营养不良是肿瘤患者的常见临床表现,但肿瘤患者所处的治疗阶段不同,代谢特征不同,所需营养物质的量和比例也有所不同。
一、围手术期患者的营养治疗――顺应规律,动态管理?
手术可导致机体发生一系列相应的创伤和应激,机体会随之产生一系列代谢改变,经历回落期、起涨期、恢复期3个动态时期,详见图1。
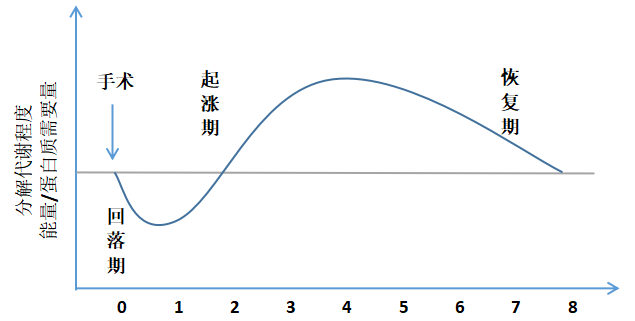
图1 代谢与围手术期的关系
1.手术前预先储备性营养(预康复)
(1)适应证
①重度营养不良患者:术前医学营养1~2周。
②中度营养不良计划实施大手术患者:术前医学营养1~2周。
③开腹大手术患者:无论营养状况如何,均推荐术前使用免疫营养5~7 d。
(2)方法
口服营养补充为首选方式,必要时使用补充性肠外营养。
(3)需要量
能量与蛋白质双达标,特别强调强化蛋白质供给[21.2 g/(kg・d)]。
2.手术后营养治疗原则
术后初期需要兼顾肠内营养和肠外营养,并尽快过渡到肠内营养,详见图2。
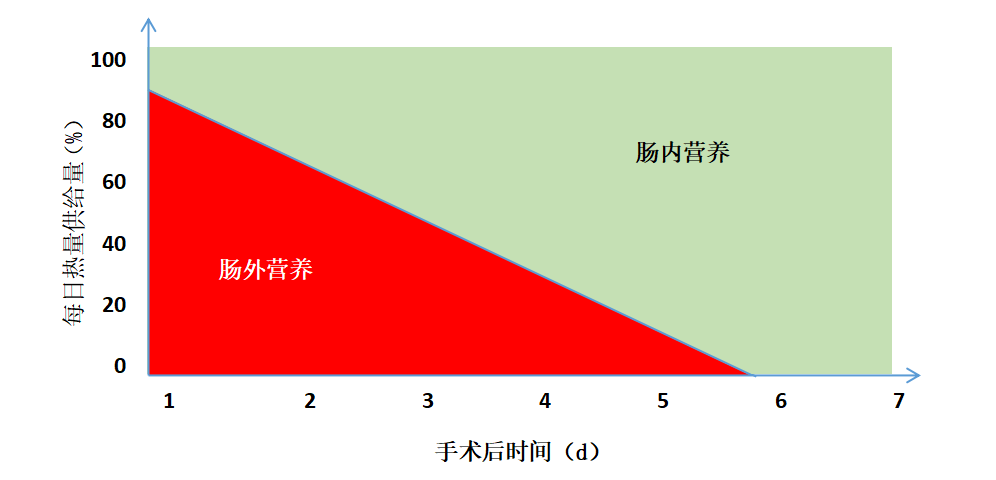
图2 术后营养情况
(1)回落期
①特征:(两低)低合成代谢、低分解代谢,合成代谢=分解代谢。
②时间:12~24 h。
③机制:条件反射性躲避反应;
④表现:(六低一高)心输出量↓、血压↓、氧消耗↓、体温↓、尿量↓、代谢率↓、血糖↑。
⑤能源:肝糖原分解。
⑥营养:核心工作是复苏,而不是营养支持。
(2)起涨期
①特征:(两高)高合成代谢、高分解代谢,分解代谢>合成代谢。
②时间:3~5 d。
③机制:回击性反应,儿茶酚胺/糖皮质激素分泌增加,导致胰高血糖素释放。
④表现:(六高一低)体温↑、心率↑、呼吸↑、代谢↑、血糖↑、白细胞↑、体重↓。
⑤能源:蛋白质分解(糖异生)及脂肪氧化(酮体),以后者为主。
⑥营养
?不迟于48 h内启动肠内营养,以肠内营养为首选;
?保证高脂肪供能比例、高蛋白质、高水溶性维生素,能量适量。
(3)恢复期
①特征:(一高一低)高合成代谢、低分解代谢,合成代谢>分解代谢。
②时间:1周至1月。
③机制:损伤修复。
④表现:(六低六高)体温↓、心率↓、呼吸↓、红细胞↓、C反应蛋白↓、疼痛↓、尿量↑、白蛋白↑、肛门排气↑、讲话↑、胃液↑、食欲↑。
⑤能源:外援供给。
⑥营养
?(二高)高蛋白、高热卡,为创伤修复提供底物;
?(三防)防止呼吸商>1.0,防止脂肪大量合成,防止体重增加过快。
二、围化疗期患者的营养治疗――面对矛盾,调整平衡
1.围化疗期营养代谢特点
化疗药物治疗的主要作用为快速增殖细胞的大量杀伤,导致细胞修复增殖,进而使细胞需求增加。而化疗药物的不良反应包括消化功能受损、食物摄入/消化/吸收障碍、营养供给减少。二者的矛盾是围化疗期营养代谢的最大特征,即化疗药物可加重营养不良,营养不良也会影响化疗药物的代谢,进而降低患者耐受性(图3)。
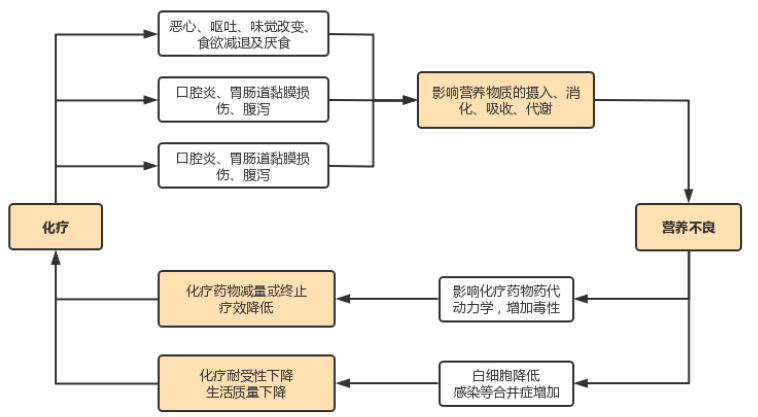
图3 化疗药物与营养素的相互作用
2.围化疗期营养治疗的原则
(1)适应证
①已存在中度营养不良的化疗患者。
②化疗严重影响摄食并预期持续时间>1周或即使中止化疗后在较长时间内仍然不能恢复足够饮食者。
③每日摄入能量<每日能量消耗60%且时间超过10 d的化疗患者。
(2)治疗目标
①提供充足的能量与营养素。
②减轻恶心、呕吐等胃肠道症状。
③保护胃肠道黏膜。
(3)方法
①遵循肿瘤患者营养总体原则。
②营养状态良好,无营养风险的化疗患者,需做好营养教育,无需常规营养治疗。
③对有营养治疗适应证的化疗患者,应尽早开始营养治疗。
④保证充足的蛋白质,每日1.0~1.5 g/kg,最高可达每天2.0 g/kg。
⑤可选择免疫营养素联合应用,调节免疫功能。
三、围放疗期患者的营养治疗――全局急晚,扶护促生
1.围放疗期营养代谢特征
放疗虽然属于局部治疗,但具有远隔效应和远期效应,患者常会出现恶心、呕吐等不良反应,进而导致营养摄入减少,出现乏力、体重减轻等机体损伤情况。
2.围放疗期营养治疗的原则
(1)适应证
①存在中度营养不良的肿瘤患者在接受放疗时需要进行营养治疗。
②放疗期间出现严重不良反应、无法正常进食或进食量明显减少的患者,应及时给予充足的营养摄入,以避免营养状态恶化和放疗中断。
(2)治疗流程
①放疗前:对营养不良的患者进行营养治疗以改善营养状况,为放射治疗做好充足的准备。
②放疗中:评估患者的营养状况及急性放射损伤,给予营养治疗,增加放射敏感性、精确性和耐受性。
③放疗后:如患者仍存在经口摄食不足,需进行家庭营养治疗。
素材来源网络,如侵删